Gelose NTM Elite
Isolamento seletivo de Micobactérias Não-Tuberculosas
A gelose NTM Elite é um meio seletivo inovador para o isolamento de Micobactérias Não-tuberculosas (NTM) de amostras respiratórias, incluindo amostras de pacientes com fibrose quística
- Fertilidade e seletividade elevadas
- Sem fase de descontaminação
- Utilizável em laboratórios de microbiologia de rotina
Precisa de mais informação?
Vastamente presentes no ambiente, as Micobactérias Não-Tuberculosas (NTM) são patogéneos oportunistas que podem causar doenças pulmonares crónicas. A M.abscessus e o complexo M.avium complex são as espécies mais frequentemente encontradas nas infeções pulmonares. Associadas a danos pulmonares progressivos, a M.abscessus é também a micobactérias mais resistente a antibióticos, extremamente difícil de tratar.(1)
Em pacientes que sofrem de Fibrose Quística, Doenças Pulmonares Obstrutivas Crónicas ou Bronquiectasia, o diagnóstico correto de infeção por NTM é essencial para ajudar os clínicos a selecionarem o tratamento adequado e implementarem as medidas apropriadas. O rastreio anual é agora altamente recomendado, e o seguimento regular em casos positivos necessário.(2)
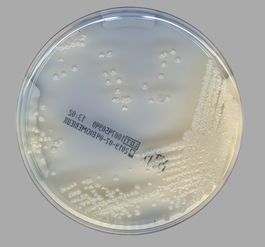
Concebido para cultura seletiva de NTM, a placa de gelose NTM Elite é a última versão industrial do meio RGM. Permite um diagnóstico fácil e melhorado comparado com o meio de cultura de Bacilos Ácido-Rápidos (AFB).
Exatidão e fluxo de trabalho melhorado
- Sem necessidade descontaminação prévia
- Elevada seletividade: 85.6% versus 18.6%*
- Fertilidade melhorada drasticamente: 95% versus 40%*
- Incubação a 30°C melhora o crescimento de NTM sem permitir o crescimento de micobactérias BSL3**
- Utilizável em laboratórios de microbiologia BSL2** em rotina
* comparado com o método de referência AFB: Meio Lowenstein Jensen associado ao meio MGIT
** BSL: Nível de biosegurança
Leitura fácil

(1) Doença pulmonar por micobactérias não-tuberbulosas - gestão clínica, necessidades não satisfeitas e perspetivas futuras.
Larsson, L. O., E. Polverino, W. Hoefsloot, L. R. Codecasa, R. Diel, S. G. Jenkins and M. R. Loebinger
Expert Rev Respir Med 2017 11(12): 977-989.
PubMed link: https://www.ncbi.nlm.nih.gov/pubmed/28967797
Journal site link : https://www.tandfonline.com/doi/abstract/10.1080/17476348.2017.1386563
(2) Recomendações consensuais da US Cystic Fibrosis Foundation e da European Cystic Fibrosis Society para o tratamento de micobactérias não tuberculosas em indivíduos com fibrose quística.
Floto, R. A., K. N. Olivier, L. Saiman, C. L. Daley, J. L. Herrmann, J. A. Nick, P. G. Noone, D. Bilton, P. Corris, R. L. Gibson, S. E. Hempstead, K. Koetz, K. A. Sabadosa, I. Sermet-Gaudelus, A. R. Smyth, J. van Ingen, R. J. Wallace, K. L. Winthrop, B. C. Marshall and C. S. Haworth
Thorax 2016 71 Suppl 1: i1-22.
PubMed link: https://www.ncbi.nlm.nih.gov/pubmed/26666259
Journal site link: https://thorax.bmj.com/content/71/Suppl_1/i1.long
| Gelose NTM Elite | ||
|---|---|---|
 |
Ref. 423144 | 20 placas x 90 mm |
ARTIGOS
- Stephenson D, et al. (Freeman Hospital). An evaluation of methods for the isolation of nontuberculous mycobacteria from patients with cystic fibrosis, bronchiectasis and patients assessed for lung transplantation. BMC Pulmonary Medicine (2019).
https://www.ncbi.nlm.nih.gov/pubmed/30665395 - Brown-Elliott BA, et al. Evaluation of a novel rapidly-growing mycobacteria medium for isolation of Mycobacterium abscessus complex from respiratory specimens from patients with bronchiectasis. Heliyon, 2019.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6820269/ - Rotcheewaphan S, et al (NIH). Performance of RGM Medium for Isolation of Non Tuberculous Mycobacteria from Respiratory Specimens from Non-Cystic Fibrosis Patients. Journal of Clinical Microbiology. February 2019 Volume 57 Issue 2.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6355514/ - Scohy A, et al. Comparison of the RGM medium and the mycobacterial growth indicator tube automated system for isolation of non-tuberculous mycobacteria from sputum samples of cystic fibrosis in Belgium. J Clin Tuberc Other Mycobact Dis. 2018.
https://www.ncbi.nlm.nih.gov/pubmed/31720403 - Plongla R, et al. (Chapel Hill NC). Evaluation of RGM Medium for Isolation of Non Tuberculous Mycobacteria from Respiratory Samples from Patients with Cystic Fibrosis in the United States. Journal of Clinical Microbiology. May 2017 Volume 55 Issue 5. 1469-1477.
https://www.ncbi.nlm.nih.gov/pubmed/28228494 - Eltringham I, et al. Comparison of mycobacterial growth indicator tube with culture on RGM selective agar for detection of mycobacteria in sputum samples from patients with cystic fibrosis. Journal of Clinical Microbiology, 2016 August.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4963527/ - Preece CL, et al. (Freeman Hospital). Evaluation of Various Culture Media for Detection of Rapidly Growing Mycobacteria from Patients with Cystic Fibrosis. Journal of Clinical Microbiology. July 2016 Volume 54 Number 7. 1797-1803.
https://www.ncbi.nlm.nih.gov/pubmed/27098962 - Preece CL, et al. (Freeman Hospital). A novel culture medium for isolation of rapidly-growing mycobacteria from the sputum of patients with cystic fibrosis. Journal of Cystic Fibrosis 15 (2016) 186-191.
https://www.ncbi.nlm.nih.gov/pubmed/26002312
RESUMOS
ECCMID 2020
- Perry J, et al. Decontamination strategies used for AFB culture significantly reduce the viability of Mycobacterium abscessus in sputum samples from patients with cystic fibrosis.
Abstract # 2188. Session: Increasing knowledge on NTMs - PS022. Poster # P0517. - Vrignaud M, et al. Compatibility of the new NTM Elite agar with MALDI-TOF for direct isolation and identification of non-tuberculous mycobacteria.
Abstract # 2646. Session: Increasing knowledge on NTMs - PS022. Poster # P0511. - Vrignaud M, et al. Performances comparison between rapidly growing mycobacteria medium for direct-isolation of non-tuberculous mycobacteria, and its industrial version.
Abstract # 2047. Session: Increasing knowledge on NTMs - PS022- Poster # P0512. - Gafsi J et al. Performance of the NTM Elite agar for the detection of non-tuberculous mycobacteria in sputum samples of patients with cystic fibrosis.
Abstract # 5277. Session: Clinical challenges and culture-based diagnostics – PS104. Poster # P2407.
O ECCMID Abstract Book 2020 está disponível gratuitamente em formato pdf no website do ESCMID.
Os resumos podem ser encontrados através do seu número.
ASM 2020
- Vrignaud M, et al. Appropriateness of Utilization of NTM Elite agar for the Diagnosis of Nontuberculous Mycobacteria Outside Biosafety Level 3 Laboratories.
Abstract # 4705.